Электроимпедансный маммограф "МЭИК"
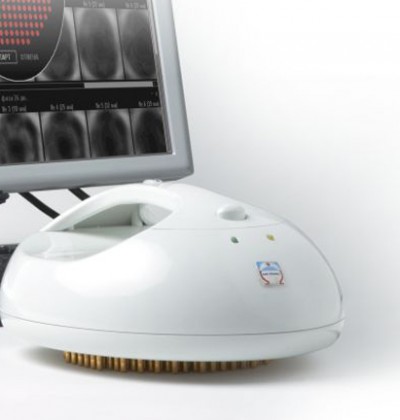
Маммограф электроимпедансный компьютерный для скринингового обследования молочной железы «МЭИК» Принцип действия прибора, это метод основанный на том, что различные биологические ткани имеют разную проводимость к электрическому току заданной частоты.
Маммограф «МЭИК»® позволяет визуализировать распределение электропроводности биологических тканей в нескольких поперечных сечениях тела пациента и обнаруживать на изображениях патологические изменения как области с аномальными значениями электропроводности.



Новости и события
Наши публикации
20 ЛЕТ УСПЕШНОЙ РАБОТЫ
 Производственно-коммерческая фирма «Современная Импедансная Медицинская техника» (ПКФ «СИМ-техника») создана в 2002 году. С момента своего образования, компания занимается разработкой, производством и реализацией современного медицинского диагностического оборудования. ПКФ «СИМ-техника» является одним из мировых лидеров в разработке и серийном производстве электроимпедансного оборудования.
Производственно-коммерческая фирма «Современная Импедансная Медицинская техника» (ПКФ «СИМ-техника») создана в 2002 году. С момента своего образования, компания занимается разработкой, производством и реализацией современного медицинского диагностического оборудования. ПКФ «СИМ-техника» является одним из мировых лидеров в разработке и серийном производстве электроимпедансного оборудования.
Одной из самых значимых и важных для здоровья женщин разработок компании является электроимпедансный маммограф «МЭИК ®», предназначенный для точного, быстрого и безопасного обнаружения патологических и непатологических заболеваний молочной железы у женщин.
За истекший период компанией освоены современные технологии и практически реализованы в мощный производственно-научный комплекс, позволяющий разрабатывать и производить электроимпедансное оборудование в необходимых объемах и в кратчайшие сроки. Постоянное развитие и совершенствование технологических процессов позволяет предприятию улучшать качество выпускаемой продукции.
Ю.А.Цофин
директор ООО ПКФ «СИМ-техника», кандидат химических наук